第4章 〜活性酸素種による生体の傷害・老化と延命効果〜
多くの生物は の
の への4電子還元(
への4電子還元( ) を利用してエネルギーを獲得しているが、その
) を利用してエネルギーを獲得しているが、その 還元過程においていくつかの中間代謝物を生じる。これらは極めて反応性が高く活性酸素と呼ばれ、生態系に種々の障害をもたらすことから、活性酸素と種々の疾患との関わりが近年注目されるところとなった。
還元過程においていくつかの中間代謝物を生じる。これらは極めて反応性が高く活性酸素と呼ばれ、生態系に種々の障害をもたらすことから、活性酸素と種々の疾患との関わりが近年注目されるところとなった。
これら活性酸素種(ROS: reactive oxygen species)による傷害は日常的に細胞内で生じているものであり、①活性酸素の生成、②抗酸化物質による消去、③損傷の修復の3つのバランスの上に生体は成り立っている。活性酸素種や酸化ストレスの老化への関与は以前から指摘されているが、中でもそれらによって生じるフリーラジカル、過酸化脂質の増加が老化の原因であるとする考え方が近年注目を集めているので、この章ではそういった内容を説明していきたい。
語注
ラジカル(フリーラジカル)…分子または原子団に不対電子を持つ化学種のこと
4.1.1 活性酸素とは
活性酸素と言われているのは狭義には酸素の1電子還元で生じるラジカルで陰イオンでもあるスーパーオキシド( )、これより派生する過酸化水素(
)、これより派生する過酸化水素( )、ヒドロキシルラジカル(
)、ヒドロキシルラジカル(  )、および励起状態の酸素である一重項酸素(
)、および励起状態の酸素である一重項酸素(  )などである。広義には脂質ペルオキシラジカル、脂質ヒドロペルラジカルなども含まれる。これらは炎症、虚血、癌化など多様な病態に深く関わっているが、老化に関しても好気的生物の宿命として活性酸素による傷害の蓄積が細胞や生体の寿命を左右しているのである。
)などである。広義には脂質ペルオキシラジカル、脂質ヒドロペルラジカルなども含まれる。これらは炎症、虚血、癌化など多様な病態に深く関わっているが、老化に関しても好気的生物の宿命として活性酸素による傷害の蓄積が細胞や生体の寿命を左右しているのである。
4.1.2 活性酸素種の生成と生体成分の傷害
細胞内での活性酸素生成源としては、①ミトコンドリア、②ホルボールエステルにより活性化された白血球、③キサンチン-キサンチン酸化酵素系の3つが主なものとして挙げられるが、後述のようにミトコンドリアが最も重要であり、老化をはじめアポトーシスにも関連していると考えられている。定常状態においても活性酸素種の生成は図1に示すような割合で抗酸化物質によってかなり抑えられた状態ではあるが確かに発生している。
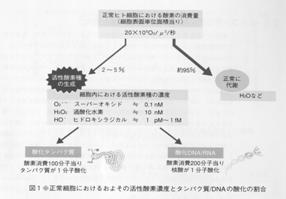 (図1)
(図1)
その結果タンパク質 やDNAの傷害も健常時においてもある一定の割合でたえず発生しているのであるが、ふだんは傷ついたタン パク質やDNAは速やかに代謝されたり修復、除去されていて細胞に障害を及ぼさない。しかしこの生成-消去-修復の3
者のバランスが崩れると細胞は障害される。老化との可能性を考える場合、消去—修復系の存在があっても障害がある割合 で蓄積される可能性がある。つまり例えばDNAは再生の際、鋳型を忠実に複製せねばならないので障害が保存されたり、とき
には増幅されてしまうのである。また逆に老化に伴って3者のバランスが崩れ細胞機能障害が起きやすくなっている場合も考えられる。
今述べたような活性酸素によるDNA損傷の蓄積はわかりやすく、老化のメカニズムとしてとても魅力的なのだが現在では次に扱うミトコンドリアにおける活性酸素生成とDNA損傷が注目されているようである。
語注
抗酸化物質…SOD、カタラーゼなどの活性酸素を消去する酵素、アルブミンなどの結合タンパク質、ビタミンCなどの低分子化合物がある。作用の面からは酵素のような活性酸素消去物質、活性酸素の捕捉、安定化をするラジカルスカベンジャーとなる物質がある。この後4.3で若干取り上げる。
4.2.1 ミトコンドリアにおける活性酸素生成と老化
ミトコンドリアは生体内で最大の活性酸素発生源であり、若くて抗酸化系とバランスが取れている間はよいが、やがてバランスが崩れたり、老化したミトコンドリアから抗酸化系では処理しきれない活性酸素が漏れ出て細胞に傷害を与える。このようなことから近年このミトコンドリアの活性化による損傷が老化の重要な原因として考えられるようになった。上に述べた他にも老化のミトコンドリア説には多くの報告があり、次にまとめてみる。
表1 老化における活性酸素-ミトコンドリア説の根拠
| ① |
酸素の90%以上がミトコンドリアで代謝
|
|
②
|
ミトコンドリアにおける活性酸素生成量と各種の動物種の寿命の間に負の相関が存在
|
|
③
|
ミトコンドリアDNA(mt-DNA)は活性酸素生成源の近傍に存在
|
|
④
|
mt-DNAは情報密度が高く、修復能が低い
|
|
⑤
|
加齢に伴ってmt-DNAの欠失や変異が増える
|
|
⑥
|
核のDNAよりもmt-DNAの方が8-OHdGが多い(※8-OHdG…DNAの酸化産物)
|
|
⑦
|
ミトコンドリア内膜は不飽和脂肪酸に富んでいて、不飽和脂肪酸は活性酸素によって過酸化など変形されやすい
|
|
⑧
|
活性酸素はミトコンドリアの転写を阻害する
|
4.2.2 摂取カロリーと寿命
さて、古くから体重や脳重量の大きな動物は長寿であることが知られ、代謝が遅い動物種ほど活性酸素発生が少ないことが報告されている。この理屈を順を追って説明してみると、①生物が生存を続けるには体温を保ち、代謝を維持していかねばならない→②体表面積が体長の2乗に比例して増えるのに対し、体重は3乗に比例して増大するため、単位体重あたりの代謝量(これを比代謝量という)が少ない動物ほど老化速度が遅い、ということになる。つまり、③代謝活性が高いと酸素消費量が増加し→④ミトコンドリアで発生する活性酸素が増大し→⑤その結果、活性酸素による組織障害や過酸化脂質の蓄積が起こる、という流れである。
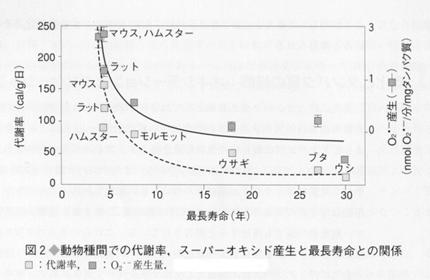
逆に言えば、代謝を低下させミトコンドリアにおける活性酸素生成を抑制すれば長寿になると考えられ、事実、図2に見られるように代謝率の小さい動物種ほど長寿であり、動物実験では低体温やいわゆる「冬眠」が寿命を延ばすことが報告されている。
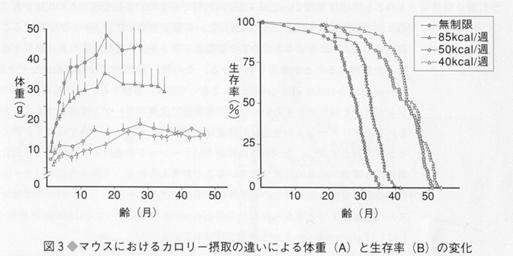
近年、ヒトとも密接に関与してミトコンドリアの酸素代謝を亢進させ、活性酸素の生成を増加させる要因の1つとしてカロリーの摂取が考えられている。図3からマウスの実験では、カロリーの摂取が多いほど短命であることがわかっている。つまりこれはカロリーが制限されると寿命が伸びる可能性を示唆しており、カロリー制限による活性酸素生成抑制との関与が考えられている。
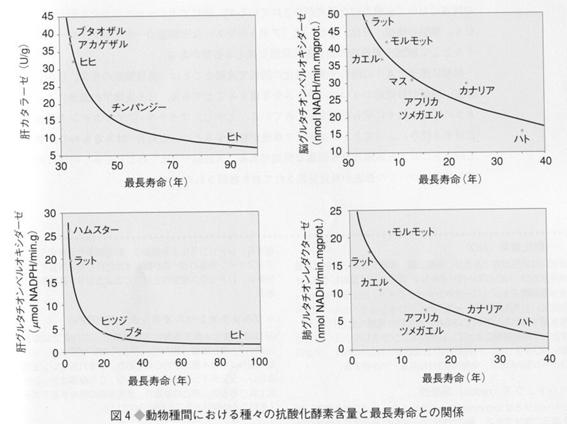
これらから完全に断定することはできないが、タンパク質あたりの抗酸化酵素が少ないことは細胞あたりの活性酸素生成が少なく、傷害も少なくなる、という一応の予想を立てることができる。
各種の生物の短命種と長命種を用いてSOD(スーパーオキシドジスムターゼ=代表的な活性酸素)と寿命の関係を測定する試みも多くなされているが、必ずしも一定の評価が定まっているようではないのでここでは取り扱わないことにする。
4.4 今後の研究の展開
老化研究は長期期間を要するため、時間の制約上(!)短命なショウジョウバエや線虫など短命な動物種を使うことが多く、ヒトの老化との関連をどう考えるかが古くからの課題となっている。
しかし、老化促進モデルマウス(senescence accelerated mouse = SAM)が京大胸部研病理学部門において約20年の歳月をかけて開発され、老化兆候の早期出現と寿命の短縮を可能としたほか、近年の分子生物学の進歩は、遺伝子の塩基配列の相同性からの関連の推測を可能にした。これらにより今後、ヒトゲノム解読のデータ利用も含め大きな進歩が期待される。
また、細胞生物学的には活性酸素を単なる細胞傷害物質として考えるのではなく、1種のシグナルという観点からも考えることができる。単にミトコンドリアを中心にアポトーシスや老化を解析するのではなく、細胞の増殖、分化、老化、死など細胞の一生をコントロールするシグナルとしてROSや細胞内の酸化還元状態を捉える必要がある。
活性酸素自体の研究としては、ヒドロキシラジカルに加えて血管拡張、神経伝達など多彩な生理作用を持つ一酸化窒素( )の研究が盛んになると言われている。
)の研究が盛んになると言われている。
活性酸素と老化との関係で重要なことは、4.1.2で述べたように活性酸素の生成、抗酸化物質の存在、損傷の修復能の3つのバランスを考慮することである。とはいえ、個体としてのヒトに対する応用をどうするのか、これからの研究が期待される。
(参考文献)
「わかる実験医学シリーズ 老化研究がわかる」編集 井出利憲(羊土社)
「季刊化学総説活性酸素種の化学」 日本化学会 (学生出版センター)
不老不死への科学



